ДИНАМИЧЕСКАЯ БИОХИМИЯ
Глава IV.8.
Обмен веществ и энергии
Метаболизм или обмен веществ - совокупность химических
реакций в организме, которые обеспечивают его веществами и энергией, необходимыми для
жизнедеятельности. В обмене веществ можно выделить два основных этапа:
подготовительный - когда поступившее алиментарным путем вещество подвергается
химическим превращениям, в результате которых оно может поступить в кровь и
далее проникнуть в клетки, и собственно метаболизм, т.е. химические превращения
соединений, проникнувших внутрь клеток.
Метаболический путь - это характер и
последовательность химических превращений конкретного вещества в организме.
Промежуточные продукты, образовавшиеся в процессе метаболизма называются
метаболитами, а последнее соединение метаболического пути - конечный продукт.
Процесс распада сложных веществ на более простые
называется катаболизмом. Так, поступающие в пищей белки, жиры, углеводы под действием ферментов
пищеварительного тракта распадаются на более простые составные части
(аминокислоты, жирные кислоты и моносахариды). При этом высвобождается энергия.
Обратный процесс, т. е. синтез сложных
соединений из более простых называется анаболизмом. Он идет с затратой
энергии. Из образовавшихся в результате пищеварения аминокислот, жирных кислот
и моносахаридов в клетках синтезируются новые клеточные белки, фосфолипиды
мембран и полисахариды.
Существует понятие амфиболизм, когда одно
соединение разрушается, но при этом синтезируется другое.
Метаболический цикл - это метаболический путь,
один из конечных продуктов которого идентичен одному из соединений, вовлеченных
в этот процесс.
Частный путь метаболизма - совокупность превращений
одного определенного соединения (углеводы или белки). Общий путь метаболизма -
когда вовлекаются два и более видов соединений (углеводы, липиды и частично
белки вовлечены в энергетический метаболизм).
Субстраты метаболизма - соединения поступающие с
пищей. Среди них выделяют основные пищевые вещества (белки, углеводы, липиды) и
минорные, которые поступают в малых количествах (витамины, минеральные
вещества).
Интенсивность метаболизма определяется потребностью
клетки в тех или иных веществах или энергии,
регуляция осуществляется четырьмя путями:
1)
Суммарная
скорость реакций определенного метаболического пути определяется концентрацией
каждого из ферментов этого пути, значением рН среды, внутриклеточной
концентрацией каждого из промежуточных продуктов, концентрацией кофакторов и
коферментов.
2)
Активностью
регуляторных (аллостерических) ферментов, которые обычно катализируют начальные
этапы метаболических путей. Большинство из них ингибируется конечным продуктом
данного пути и этот вид ингибирования называется "по принципу обратной
связи".
3)
Генетический
контроль, определяющий скорость синтеза того или иного фермента. Яркий пример -
появление в клетке индуцибельных ферментов в ответ на поступление
соответствующего субстрата.
4)
Гормональная
регуляция. Ряд гормонов способны активировать или ингибировать многие ферменты
метаболических путей.
Живые организмы представляют собой термодинамически неустойчивые
системы. Для их формирования и функционирования необходимо непрерывное
поступление энергии в форме, пригодной для многопланового использования. Для
получения энергии практически все живые существа на планете приспособились
подвергать гидролизу одну из пирофосфатных связей АТФ. В связи с этим одна из
главных задач биоэнергетики живых организмов это восполнение использованных АТФ
из АДФ и АМФ.
Основной источник энергии в клетке - окисление
субстратов кислородом воздуха. Этот процесс осуществляется тремя путями:
присоединением кислорода к атому углерода, отщеплением водорода или потерей
электрона. В клетках окисление протекает в форме последовательного переноса
водорода и электронов от субстрата к кислороду. Кислород играет в этом случае
роль восстанавливающегося соединения (окислителя). Окислительные реакции
протекают с высвобождением энергии. Для
биологических реакций характерны сравнительно небольшие изменения энергии. Это
достигается за счет дробления процесса окисления на ряд промежуточных стадий,
что позволяет запасать ее небольшими порциями в виде макроэргических соединений
(АТФ). Восстановление атома кислорода при взаимодействии с парой протонов и
электронов приводит к образованию молекулы воды.
Тканевое дыхание
Это процесс потребление клетками тканей организма
кислорода, который участвует в биологическом окислении. Такой вид окисления
называют аэробным окислением. Если конечным акцептором в цепи переноса
водорода выступает не кислород, а другие вещества (например пировиноградная
кислота), то такой тип окисления называют анаэробным.
Т.о. биологическое окисление - это дегидрирование
субстрата с помощью промежуточных переносчиков водорода и его конечного
акцептора.
Дыхательная цепь (ферменты тканевого
дыхания) - это переносчики протонов и электронов от окисляемого субстрата на
кислород. Окислитель - это соединение, способное принимать электроны. Такая
способность количественно характеризуется окислительно-восстановительным потенциалом
по отношению к стандартному водородному электроду, рН которого равен 7,0. Чем
меньше потенциал соединения, тем сильнее его восстанавливающие свойства и
наоборот.
Т. о. любое соединение может отдавать электроны
только соединению с более высоким окислительно-восстановительным потенциалом. В
дыхательной цепи каждое последующее звено имеет более высокий потенциал, чем
предыдущее.
Дыхательная цепь состоит из:
1.
НАД
- зависимой дегидрогеназы;
2.
ФАД-
зависимой дегидрогеназы;
3.
Убихинона
(КоQ);
4.
Цитохрмов
b, c, a+a3 .
НАД-зависимые
дегидрогеназы. В качестве кофермента содержат НАД и НАДФ.
Пиридиновое кольцо никотинамида способно присоединять электроны и протоны
водорода.
ФАД и ФМН-зависимые
дегидрогеназы содержат в качестве кофермента фосфорный эфир витамина В2 (ФАД).
Убихинон (КоQ) отнимает водород у флавопротеидов
и превращается при этом в гидрохинон.
Цитохромы - белки хромопротеиды,
способные присоединять электроны, благодаря наличию в своем составе в качестве простетических
групп железопорфиринов. Они принимают электрон от вещества, являющегося немного
боле сильным восстановителем, и передают его более сильному окислителю. Атом
железа связан с атомом азота имидазольного кольца аминоксилоты гистидина с
одной стороны от плоскости порфиринового цикла, а с другой стороны с атомом
серы метионина. Поэтому потенциальная способность атома железа в цитохромах к
связыванию кислорода подавлена.
В цитохроме с порфириновая
плоскость ковалентно связана с белком через два остатка цистеина, а в цитохромах b и а,
она ковалентно не связано с белком.
В цитохроме а+а3
(цитохромоксидазе) вместо протопорфирина содержатся порфирин А,
который отличатся рядом структурных особенностей. Пятое координационное
положение железа занято аминогруппой, принадлежащей остатку аминосахара,
входящего в состав самого белка.
В отличии от гема гемолгобина атом железа в
цитохромах может обратимо переходить из двух в трехвалентное состояние это обеспечивает транспорт электронов (См.
подробнее приложение 1 "Атомная и электронная структура гемопротеинов
").
Механизм работы электронтранспортной
цепи
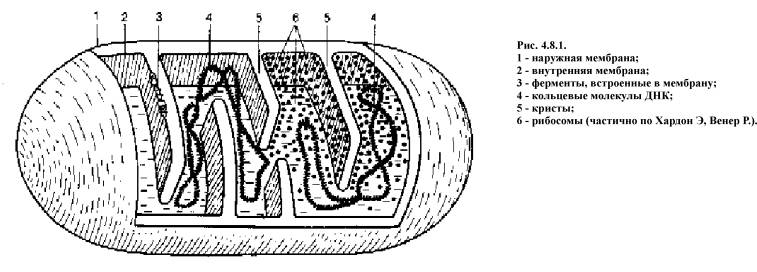
Наружная мембрана митохондрии (рис. 4.8.1)
проницаема для большинства мелких молекул и ионов, внутренняя почти для всех
ионов (кроме протонов Н) и для большинства незаряженных молекул.
Все вышеперечисленные компоненты дыхательной цепи
встроены во внутреннюю мембрану. Транспорт протонов и электронов по дыхательной
цепи обеспечивается разностью потенциалов между ее компонентами. При этом каждое
увеличение потенциала на 0,16 В освобождает энергию, достаточную для синтеза
одной молекулы АТФ из АДФ и Н3РО4. При потреблении одной
молекулы О2 образуется 3 АТФ.
Процессы окисления и образования АТФ из АДФ и
фосфорной кислоты т.е. фосфорилирования протекают в митохондриях. Внутренняя
мембрана образует множество складок - крист. Пространство органиченное
внутренней мембраной - матриксом. Пространство между внутренней и наружной
мембранами называется межмембранным.
Такая молекула содержит в себе три макроэргических
связи. Макроэргической или богатой энергией называют химическую связь,
при разрыве которой высвобождается более 4 ккал/моль. При гидролитическом
расщеплении АТФ до АДФ и фосфорной кислоты высвобождается 7,3 ккал/моль. Ровно
столько же тратится для образования АТФ из АДФ и остатка фосфорной кислоты и
это один из основных путей запасания энергии в организме.
В процессе транспорта электронов по дыхательной цепи
высвобождается энергия, которая тратится на присоединение остатка фосфорной
кислоты к АДФ с образованием одной молекулы АТФ и одной молекулы воды. В
процессе переноса одной пары электронов по дыхательной цепи высвобождается и
запасается в виде трех молекул АТФ 21,3 ккал/моль. Это составляет около 40 %
высвободившейся при электронном транспорте энергии.
Такой способ запасания энергии в клетке называется окислительным
фосфорилированием или сопряженным фосфорилированием.
Молекулярные механизмы этого процесса наиболее полно
объясняет хемоосмотическая теория Митчелла, выдвинутая в 1961 году.
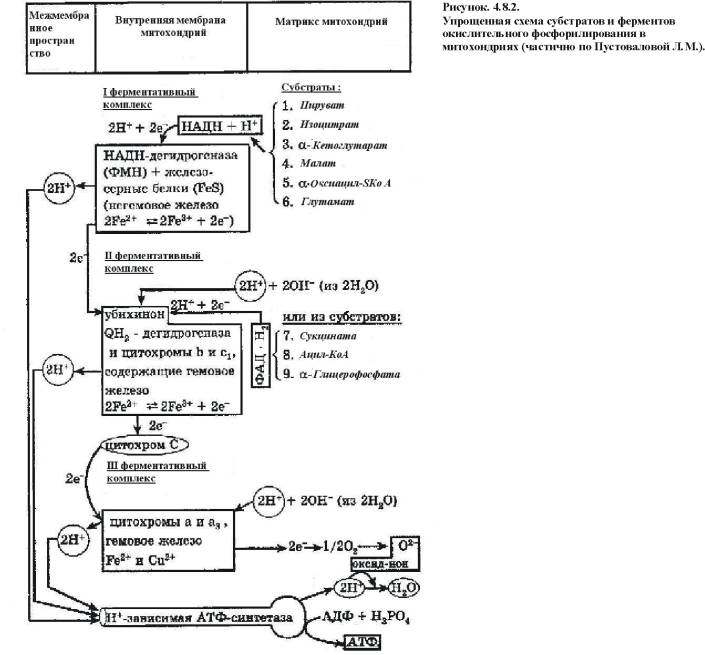
Механизм окислительного
фосфорилирования (рис.4.8.2.):
1)
НАД-зависимая
дегидрогеназа расположена на матриксной поверхности внутренней мембраны
митохондрий отдает пару электронов водорода на ФМН-зависимую дегидрогеназу. При
этом из матрикса пара протонов переходит также на ФМН и в результате образуется
ФМН Н2. В это время пара протонов, принадлежащих НАД выталкивается в
межмембранное пространство.
2)
ФАД-зависимая
дегидрогеназа отдает пару электронов на КоQ а пару протонов выталкивает
в межмембранное пространство. Получив электроны КоQ принимает из матрикса пару
протонов и превращается в КоQ Н2.
3)
КоQ Н2
выталкивает пару протонов в межмембранное пространство, а пара электронов
передается на цитохромы и далее на кислород с образованием молекулы воды.
В итоге при переносе пары
электронов по цепи из матрикса в межмембранное пространство перекачивается 6 протонов (3 пары), что
ведет к созданию разницы потенциалов и разницы рН между поверхностями
внутренней мембраны.
4)
Разница
потенциалов и разница рН обеспечивают движение протонов через протонный канал
обратно в матрикс.
5)
Такое
обратное движение протонов ведет к активации АТФ-синтазы и синтезу АТФ из АДФ и
фосфорной кислоты. При переносе одной пары электронов (т.е. трех пар протонов)
синтезируется 3 молекулы АТФ (рис. 4.7.3.).
Разобщение процессов дыхания и
окислительного фосфорилирования происходит если протоны начинают проникать через
внутреннюю мембрану митохондрий. В этом случае выравнивается градиент рН и
исчезает движущая сила фосфорилирования. Химические вещества - разобщители
называются протонофорами, они способны переносить протоны через мембрану. К
таковым относятся 2,4 -динитрофенол,
гормоны щитовидной железы и др. (рис. 4.8.3.).
Образовавшаяся АТФ из матрикса в цитоплазму
переносится ферментами транслоказами, при этом в обратном направлении в матрикс
переносится одна молекула АДФ и одна молекула фосфорной кислоты. Понятно, что
нарушение транспорта АДФ и фосфата тормозит синтез АТФ.
Скорость окислительного фосфорилирования зависит в
первую очередь от содержания АТФ, чем быстрее она расходуется, тем больше
накапливается АДФ, тем больше потребность в энергии и следовательно активнее
идет процесс окислительного фосфорилирования. Регуляцию скорости окислительного
фосфорилирования концентрацией в клетке АДФ называют дыхательным контролем.

ЛИТЕРАТУРА К ГЛАВЕ IV.8.
1.
Бышевский А. Ш., Терсенов О. А. Биохимия для врача // Екатеринбург: Уральский
рабочий, 1994, 384 с.;
2.
Кнорре Д. Г., Мызина С. Д. Биологическая химия. – М.: Высш. шк. 1998, 479 с.;
3.
Ленинджер А. Биохимия. Молекулярные основы структуры и функций клетки // М.:
Мир, 1974, 956 с.;
4.
Пустовалова Л.М. Практикум по биохимии // Ростов-на Дону: Феникс, 1999, 540 с.;
5.
Степанов В. М. Молекулярная биология. Структура и функции белков // М.: Высшая
школа, 1996, 335 с.;
6.
Скулачев В. П. Энергетика биологических мембран // М.: Наука, 1989, 565 с.;
7.
Карякин А. В., Арчаков А. И. Межмембранный перенос электронов // Успехи
современной биологии, 1981, Т. 91, вып. 1, с. 74-89;
8.
Методы биохимических исследований (липидный и энергетический обмен). Под ред.
М.И.Прохоровой // Л.: Изд-во Ленинградского университета, 1982. - 327 с.